Hidróxido de amonio
El hidróxido de amonio, mejor conocido como amoníaco líquido, es una mezcla de agua y gas amoníaco que tiene múltiplos usos. No tiene color y su olor es muy fuerte. Se encuentra en estado natural en el medio ambiente, así como en el cuerpo humano, donde cumple funciones como las de sintetizar proteínas. Industrialmente se produce con varios fines. Para la agricultura, limpieza del hogar y medicinal, entre otros. Este compuesto químico debe ser usado con precaución, ya que una exposición inadecuada es dañina para la salud.
¿Qué es el hidróxido de amonio?
El hidróxido de amonio es un compuesto químico que se genera al diluir gas amoníaco en agua. También se le denomina como amoníaco líquido o amoníaco. Se halla en el ambiente natural en plantas, animales y en los humanos. También se crea de forma industrial para diversos usos.
Características
- Se presenta en estado líquido
- Incoloro
- No se puede aislar
- Olor agudo y fuerte
- Es corrosivo (disuelve cobre y zinc)
- Posee una densidad de 0,90 g/cm3 a 25 ºC.
- Tiene un sabor acre, desagradable.
Fórmula y nomenclatura
La fórmula molecular del Hidríxido de Amonio es NH4OH o H5NO
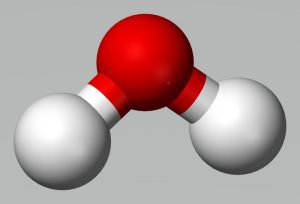
Estructura
Su estructura se compone de una “solución acuosa de gas amoníaco”. En el líquido su estructura no está definida sino por una habilidad circunstancial de iones “NH4+ y OH– solvatados por las moléculas de agua”. Su PH es: 11,6 (solución 1 N); 11,1 (solución 0,1 N) y 10,6 (solución 0,01 N).
Propiedades físicas
- Alcanza un punto de ebullición a los 38 ºC (25%).
- La solubilidad es posible solamente en solución acuosa.
- La solubilidad en el agua es miscible en proporciones ilimitadas.
- Su densidad va de 0,90 g/cm3 a 25 ºC.
Propiedades químicas
- La constante de disociación del hidróxido de amonio es: pKb = 4,767; Kb = 1,71 x 10-5 a 20 ºC; y pKb = 4,751; Kb = 1,774 x 10-5 a 25 º C.
- Un alza en la temperatura eleva de forma casi imperceptible la basicidad del hidróxido de amonio.
- Su concentración es de hasta aproximadamente un 30%, para los iones NH4+ y OH–.
- Cuando se encuentra a temperaturas que están muy por debajo del 0ºC, y cuando además alrededor hay inmensa presión, como las que se hallan los núcleos de lunas heladas en espacio, el agua y el amoniaco se congelan
Reactividad del hidróxido de amonio
- Es posible que reaccione violentamente con ácidos intensos como ácido sulfúrico, ácido clorhídrico y ácido nítrico. También resulta agresivo al combinarse con los halógenos y el sulfato de dimetilo.
- Reacciona con varios metales como plomo, plata, zinc y cobre. Igualmente, lo hace con las sales de esos metales al generar mezclas explosivas y la liberación del gas hidrógeno (inflamable).
- Por su efecto corrosivo no se usa con aluminio y cobre, ni con metales galvanizados.
- Reacciona produciendo amoniaco gaseoso al combinarse con bases como los hidróxidos de potasio o sodio que son muy fuertes.
Hidróxido de amonio en otros planetas
Científicos han comprobado que las nubes del planeta Júpiter están compuestas por hidróxido de amonio en soluciones diluidas. A pesar de ello, sondas espaciales han fallado en su búsqueda de agua en esas formaciones de nubes. Existe frustración al respecto, pues tras conocer que allí se evidencia la presencia de cristales de NH4OH anhidros, se esperaba encontrar agua.
Cómo se produce en las industrias
Las industrias que generan amoniaco lo obtiene a través de un método llamado Haber-Bosch. Este consiste en hacer reaccionar los gases de hidrógeno y nitrógeno, tras usar óxido de potasio, ión férrico y óxido de aluminio como catalizadores. Se somete a altas temperaturas y presión, para tener un rendimiento de 10 a 20 por ciento. Tras la reacción se obtiene amoníaco que, a su vez, luego de sufrir un proceso de oxidación se producen nitratos y nitritos. Con estos dos últimos se obtienen nitrato de amonio y ácido nítrico, de amplio uso en la fertilización.
Hidróxido de amonio natural
El hidróxido de amonio y el amoníaco se hallan de manera natural y común en los suelos, en el agua y en el aire del planeta Tierra. Igualmente, está presente en la flora y fauna, así como en los seres humanos. El nitrógeno es fundamental para la subsistencia de los animales y las plantes y este elemento se genera del amoníaco. En el cuerpo humano también se produce amoníaco. Este se origina en los tejidos y órganos, así como de algunas bacterias que se encuentran en el intestino y que resultan beneficiosas para la salud.
Funciones del amoníaco
Una de las labores importantes del amoníaco en los seres vivos es la de sintetizar las proteínas. Éstas se componen de una veintena de aminoácidos distintos. Las plantas los sintetizan, en su mayoría, con ayuda del nitrógeno atmosférico, pero los animales no. El cuerpo humano puede sintetizar algunos y otros simplemente pasan intactos luego de ser consumidos. Sin embargo, los aminoácidos que sintetiza lo hacen gracias a la presencia de microrganismos en el tracto gastrointestinal gracias a la acción de iones de amoníaco. Además, el amoníaco logra que el pH corporal se encuentre equilibrado.
Inocuidad en su empleo para procesar alimentos
La Food and Drug Administration (Administración de Drogas y Alimentos) señala en su normativa que el hidróxido de amonio (y otros preparados que poseen amoníaco) se reconoce como “inocuo” o “GRAS” cuando es empleado como agente de control del pH, leudante y para el acabado de superficie al procesar alimentos en las industrias. La única limitación es que el proceso se lleve a cabo con los pasos de fabricación actuales.
Usos del hidróxido de amonio
En los alimentos
- Se emplea en forma de aditivo en varios alimentos procesados para actuar como leudante, para controlar el pH y para acabados en la superficie de los alimentos.
- Se usa como antimicrobiano en alimentos cárnicos, ya que elimina bacterias, entre ellas la E. coli. El hidróxido de amonio obstaculiza el crecimiento de bacterias en el ganado, tras su efecto regulador del pH en el intestino del animal, que es donde aparece la E. coli.
- La variedad de alimentos en los que se utiliza el hidróxido de amonio es amplia. Entre ellos se encuentran los que se hornean, caramelos, pudines, quesos y chocolates.
Usos medicinales
- Se usa de manera externa en la piel para tratar picadas y mordeduras de insectos o animales.
- Sirve como antiácido, antiflatulento (expulsión de gases) y otros trastornos del sistema digestivo.
- Su empleo tópico actúa como rubefaciente en dolores musculares y de huesos agudos y crónicos.
Uso en la agricultura
- No se emplea directamente en las plantas, pero si tiene una función como fertilizante de los sembradíos.
- El nitrógeno atmosférico produce el amoníaco, luego se conduce refrigerado a los sitios donde se empleará.
- El suelo es inyectado con amoníaco presurizado. Allí reacciona con el agua edáfica y se convierte en amonio (NH4+). También se genera hidróxido de amonio. Ambos compuestos originan nitrógeno, éste junto con el potasio y el fósforo nutren las plantas y resultan fundamentales para que crezcan adecuadamente.
Usos industriales y más
- Aditivo para pinturas
- Agente plastificante
- Se añade a tintes para teñir el cabello
- Para tratar aguas residuales (antimicrobiano)
- Purificante del agua de piscinas
- Como limpiador de productos comerciales e industriales
- Producción de jabones, detergentes y tintas.
Riesgos
- Ocasiona irritación y /o daño ocular en contacto directo
- En altas concentraciones puede irritar y quemar la piel
- Si es inhalado producirá irritación de las vías respiratorias, tos, falta de aire o asfixia. Si la exposición es continua puede infectar los bronquios o irritar los pulmones.
- Estar en contacto con un grado alto de concentración de hidróxido de amonio puede provocar edema pulmonar.
- Otros síntomas de una exposición elevada y tóxica pueden ser desmayos, baja presión arterial, pérdida de la visión, sibilancias, dolor de garganta, vómitos y heces sanguinolentas.
- El hidróxido de amonio no es inflamable, pero si ocurre un incendio se crearán gases de amoníaco que pueden explotar y agravar el suceso.
- Lamentablemente, el hidróxido de amonio se emplea en la producción (contra ley) de metanfetaminas, sustancias altamente nocivas para la salud.
¿Cómo citar este artículo?
Castro Del Valle, Laura Isabel. (2020). Hidróxido de amonio. Recuperado el 3 mayo, 2025, de Euston96: https://www.euston96.com/hidroxido-de-amonio/