Ley de Charles
Es bastante interesante que muchas sustancias diferentes se comporten exactamente igual. La explicación aceptada, que James Clerk Maxwell planteó alrededor de 1860, es que la cantidad de espacio que ocupa un gas depende puramente del movimiento de las moléculas de gas. En condiciones normales, las moléculas de gas están muy lejos de sus vecinos, y son tan pequeñas que su propio volumen es insignificante. La ley de Charles es una ley de gas que establece que los gases se expanden cuando se calientan. La ley también se conoce como la ley de los volúmenes.
Temas relacionados
Ecuación de continuidad, ley de Avogadro, ley de Boyle, ley de Gay-Lussac, ley de los gases ideales
¿Qué es la ley de Charles?
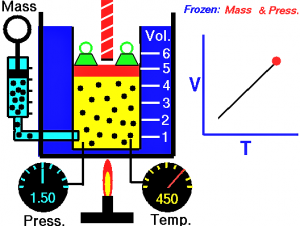
La ley de Charles es una ley que nos dice que cuando la cantidad de gas y de presión se mantienen constantes, el cociente que existe entre el volumen y la temperatura siempre tendrán el mismo valor.
En qué consiste la ley de Charles
La ley de Charles es una de las leyes que se encuentra relacionada con los gases. Consiste en la relación que existe entre el volumen y la temperatura de una cierta cantidad de gas ideal, el cual se mantiene a una presión constante, por medio de una constante de proporcionalidad que se aplica de forma directa. Jacques Charles dice que para una determinada suma de gas a una presión constante, al aumentar la temperatura, el volumen del gas aumenta y al disminuir la temperatura, el volumen del gas disminuye porque la temperatura se encuentra directamente relacionada con la energía del movimiento que tienen las moléculas del gas. Así que, para cierta cantidad de gas a una presión dada, se dará una mayor velocidad de las moléculas y mayor volumen del gas.
Historia
La ley de Charles fue promulgada por Jacques Alexandre Charles un reconocido físico y químico de origen francés. Fue profesor de física en el Conservatorio de Artes y Oficios de París y con los hermanos Robert, construyó el primer globo propulsado por hidrógeno. En 1787 descubrió la relación que existía entre el volumen y la temperatura de un gas que se encontraba con una presión constante. En 1802 publicó sus resultados, que fueron conocidos como «ley de Charles y Gay-Lussac».
Quién la propuso
La ley toma su nombre del científico e inventor francés Jacques Charles, quien la formuló en la década de 1780. La parte irónica de la historia es que Charles nunca publicó el trabajo por el cual es recordado, ni fue el primero ni el último en hacer este descubrimiento. De hecho, Guillaume Amontons había hecho el mismo tipo de experimentos 100 años antes, y fue Joseph Gay-Lussac en 1808 quien hizo las mediciones definitivas y publicó resultados que muestran que cada gas que probó obedeció esta generalización.
Enunciado de la ley de Charles
La ley de Charles establece el siguiente postulado: «A presión constante, el volumen que ocupa una muestra de gas es directamente proporcional a las temperaturas absolutas que soportan»
Fórmula
De acuerdo con el enunciado de la ley, ésta se puede expresarse matemáticamente de la siguiente manera:
V1·T2 = V2·T1
En donde :
- V= se usa para representar el Volumen.
- T= con esta letra representamos la Temperatura
Experimentos
En un día frío cuando se sale con un globo de helio el globo se desmorone. Pero cuando se regrese a la temperatura cálida, el globo volverá a su forma original. De acuerdo con la ley de Charles, esta situación se da porque un gas, en este caso, helio, ocupa más espacio cuando está caliente.
Una antorcha que se usa para calentar las moléculas de aire dentro del globo, éstas se mueven más rápido y se dispersan dentro del espacio. El gas dentro del globo ocupa más espacio, volviéndose menos denso que el aire que lo rodea. Por lo que el aire caliente dentro del globo se eleva debido a su densidad reducida y hace que el globo flote.
Los termómetros pop-up funcionan con la ley de Charles. El termómetro se coloca en el pavo y conforme la temperatura aumenta y el pavo se cocina, el aire en el termómetro se expande para hacer estallar el émbolo. El termómetro está calibrado para cuando alcance la temperatura interna correcta, la tapa del termómetro se dispare, indicando que el pavo está listo.
Cuando se juega ping pong, la bola puede estar abollada. Si se calienta agua suavemente mientras revuelve y se coloca la bola dentro, el aire dentro de la bola se expandirá a medida que se caliente. El aire en expansión empujará la abolladura y restaurará la redondez de la bola.
Aplicaciones de la ley de Charles
La ley de Charles puede se utilizada en las siguientes aplicaciones:
- Globos aerostáticos
- Bolsas de aire
- Olla de presión.
Importancia
Su importancia radica en que de acuerdo con esta ley, los gases se expanden al calentarse. Dado que la masa de gas permanece igual, el número de moléculas por unidad de volumen disminuye al calentarse. En otras palabras, nos explica que el aire caliente es menos denso que el aire frío. esto permite que los globos de aire caliente se eleven desplazando el aire más frío de la atmósfera.
Ejemplos
Un ejemplo de la ley de Charles ya resuelto es el siguiente:
- A 1,5 atmósferas y 25 °C el volumen de un gas es de 600 cm3, si la presión permanece inalterable ¿Cuál será el volumen del gas a 20 °C?
Primer paso: se deben identificar los datos que se dan en el enunciado
P1= 1,5 atm (cte)
T1= 25°C
V1= 600 cm3
T2= 20 °C
Segundo paso: saber cuál es la incógnita.
V2= ?
Tercer paso: se debe de despejar V2 de la expresión: V1·T2 = V2·T1, quedando así:
V2= V1·T2
Cuarto paso: transformar °C a K, de la siguiente manera:
T1: K= °C + 273 T2: K= °C + 273
K= 25 + 273= 298 K K= 20 + 273= 293 K
Por último se sustituyen los valores y se realiza el cálculo matemático.
V2= 600 cm3 . 293 K
298 K
Se cancelan las unidades (Kelvin) y se obtiene el resultado: V2= 589,93 cm3
¿Cómo citar este artículo?
Briceño V., Gabriela. (2018). Ley de Charles. Recuperado el 4 mayo, 2025, de Euston96: https://www.euston96.com/ley-de-charles/