Modelo atómico de Sommerfeld
Arnold Sommerfeld fue un famoso físico y matemático atómico conocido principalmente por su trabajo en teoría atómica en el campo de la mecánica cuántica y por ser mentor de la mayor cantidad de Premios Nobel de Física que cualquier otro físico. Sommerfeld descubrió que en algunos átomos, los electrones lograban alcanzar velocidades muy cercanas a la velocidad de la luz por lo que optó por basar su análisis en la teoría relativista. Esta decisión estuvo llena de intrigas y polémicas en la época, debido a que la teoría de la relatividad aún no había sido aceptada en la comunidad científica.
¿Qué es el modelo atómico de Sommerfeld?
El modelo atómico de Sommerfeld es una mejor versión del modelo de Bohr, que nos explica la forma en la que se comportan los electrones por medio de diferentes niveles de energía que existen dentro del átomo dando origen a la modelización del átomo.
En qué consiste el modelo atómico de Sommerfeld
El modelo atómico de Sommerfeld consiste en la explicación del comportamiento de los electrones, afirmando que dentro de un mismo nivel de energía podían existir diferentes subniveles de energía, lo que provocada que se dieran diferentes variaciones de energía en un mismo nivel. Explicaba además que las velocidades que tenían los electrones llegaban a ser cercanas a la velocidad de la luz, razón por la cual estudio los electrones desde una perspectiva relativista.
Realizó dos modificaciones básicas, una era que los electrones podían describir órbitas cuasi-elípticas, y la otra que los electrones poseían velocidades relativistas. De acuerdo con su modelo, los electrones se encontraban girando únicamente de forma circular. Una órbita céntrica dio lugar a un nuevo número cuántico el cual se llamó número cuántico Azimutal, y que delimitaría la forma de los orbitales, y se representaría con la letra l, tomando valores variables desde 0 hasta n-1.
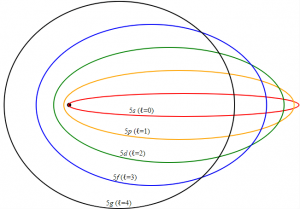
De esta manera las órbitas según el modelo atómico de Sommerfeld son:
- l=0 serían los que luego se conocerían con el nombre de como orbitales S.
- l=1 se llamaría orbital 2p u orbital principal.
- l=2 se conocería como d, u orbital difuso.
- L=3 sería el orbital llamado f o fundamental.
Características
Las principales características del modelo atómico de Sommerfeld son las siguientes:
- Buscó la forma de perfeccionar el modelo atómico de Bohr realizando algunas modificaciones.
- Postulaba que el núcleo del átomo no se encontraba inmóvil sino que por el contrario se podía mover en el centro del sistema.
- Se propuso en el modelo que las órbitas del electrón podían ser circulares y elípticas.
- Se introdujo en número cuántico secundario mejor conocido como azimutal.
- Es considerado como una generalización del modelo atómico de Bohr.
- En su modelo los electrones se encontraban en órbitas circulares alrededor del núcleo, sin irradiar ningún tipo de energía.
- Únicamente se encontraban habilitadas las órbitas en donde el momento angular del electrón cumpliera con ciertas características.
- La energía que se libera cuando un electrón desciende de una órbita a otra se producía en forma de energía luminosa.
Postulados del modelo atómico de Sommerfeld
Este modelo postula lo siguiente:
- Dentro de un mismo nivel energético (n) hay subniveles
- No existen únicamente órbitas circulares sino que también pueden existir órbitas de forma elíptica que son determinadas por el número cuántico azimutal (l) que toma valores desde 0 a n-1:
- l = 0 → forma el orbital s
- l = 1 → forma el orbital p
- l = 2 → forma el orbital d
- l = 3 → forma el orbital f
- Adapta el modelo de Bohr a la mecánica relativista ya que los electrones se mueven a velocidades cercanas a las de la luz.
- Para Sommerfeld, el electrón es una corriente eléctrica.
Aportaciones
El principal aporte de Sommerfeld fue el llegar a la conclusión de la diferencia de energía que hay entre los electrones, sin importar que estos estuviesen en un mismo nivel energético, era ocasionada a la existencia de subniveles energéticos dentro de cada nivel.
Sommerfeld se basó en la Ley de Coulomb para poder asegurar que si un electrón era sometido a una fuerza inversamente proporcional al cuadrado de la distancia, la trayectoria descrita debería ser elíptica y que no tenía que ser siempre de forma circular.
Utilizó la teoría de la relatividad de Einstein para tratar de forma diferente a los electrones, y poder de esta forma evaluar su comportamiento en función de las velocidades alcanzadas por dichas partículas fundamentales.
Qué problemas presenta el modelo atómico de Sommerfeld
El principal problema que presentaba el modelo atómico de Sommerfeld era que tomaba una partícula con una trayectoria determinada en torno al núcleo, sin embargo, la adecuada concepción de la trayectoria de los electrones en el átomo es obsoleta. Además, el modelo no logró explicar la forma de emisión de las órbitas elípticas, y únicamente trabajó con las órbitas circulares.
Importancia
Sommerfeld hizo importantes contribuciones en la teoría matemática de la difracción. Se considera que su contribución más importante fue su modelo atómico. En 1915, Sommerfeld consideró la existencia de órbitas elípticas además de la órbitas circulares del modelo de Bohr y tomó en consideración que en algunos átomos los electrones se podían mover a velocidades relativistas.
¿Cómo citar este artículo?
Briceño V., Gabriela. (2018). Modelo atómico de Sommerfeld. Recuperado el 5 enero, 2025, de Euston96: https://www.euston96.com/modelo-atomico-sommerfeld/