Principio de Le Châtelier
El principio de Le Châtelier es una observación que se realiza sobre los equilibrios químicos que se dan en las diferentes reacciones. Este principio establece que los cambios que se producen en la temperatura, presión, volumen o concentración de un sistema resultarán en cambios que pueden ser predecibles y opuestos en el sistema para lograr un nuevo estado de equilibrio. El principio de Le Châtelier se puede utilizar en la práctica para comprender las condiciones de reacción que favorecerán una mayor formación de productos. Esta idea fue descubierta y formulada independientemente por Henri Louis Le Chatelier y Karl Ferdinand Braun, en el año 1888.

Temas relacionados
Equilibrio químico, termoquímica
¿Qué es el principio de Le Châtelier?
Es un principio que establece que, si un sistema de equilibro es sometido a un determinado cambio en las condiciones, éste se desplazará a una posición nueva para contrarrestar el efecto que causo su desplazamiento y para recuperar el equilibrio.
En qué consiste el principio de Le Châtelier
El principio de Le Châtelier consiste en un principio que nos dice que un estado de equilibrio químico se mantiene de la misma manera siempre y cuando no se alteren las condiciones que tenga el sistema. Cuando se hace alguna modificación de algún parámetro, como por ejemplo, la presión, la temperatura o la concentración de algunas de sus partes, este entonces se traslada en una determinada dirección ya sea hacia los reactivos o hacia los productos con el objetivo de poder alcanzar un nuevo estado de equilibrio.
El principio también nos dice que cuando una reacción que está en equilibrio sufre de una alteración en sus condiciones, las proporciones de los reactivos y de los productos logran ajustarse de manera que consiguen minimizar el efecto que produce la alteración. El principio toma en cuenta los efectos en la concentración cuando en las variaciones que se dan en las concentraciones de especies que participan del equilibrio químico pueden llegar a alterar las especies. El principio de Le Châtelier explica esta situación tomando en cuenta que, para un sistema que se encuentra en equilibrio químico, la variación de la concentración de uno de los componentes constituye en sí una fuerza.
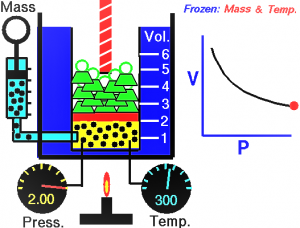
Observa también los efecto de la presión ya que éstos pueden llegar a ejercen un efecto en la posición de equilibrio. Cuando se afecta la presión, la reacción puede moverse al lado que tenga una menor cantidad de moles de gas para reducir la elevación de la presión. Cuando esta presión disminuye, entonces la reacción se mueve al lado que tenga más cantidad de moles de gas para evitar la reducción de la presión. Una vez alcanzado el equilibrio, el aumento en la presión produce una reducción de los moles de gas que están presentes y por lo tanto, la presión.
Con respecto a los efectos en la temperatura, el principio de Le Châtelier nos dice que si en el sistema de la reacción la temperatura es elevada, la reacción se moverá al lado que absorbe el calor, y si la temperatura disminuye, la reacción se irá hacia el lado que irradie calor.
Enunciado
El principio de Le Châtelier, principio que fue postulado en el año de 1884 por Henri-Louis Le Châtelier, un importante químico industrial francés, establece que:
“Si se presenta una perturbación externa sobre un sistema en equilibrio, el sistema se ajustará de tal manera que se cancele parcialmente dicha perturbación en la medida que el sistema alcanza una nueva posición de equilibrio”.
En su enunciado, la palabra perturbación se refiere a los cambios de concentración, presión, volumen o temperatura que pueden llegar a provocar una alteración en el estado de equilibrio que tiene un sistema. El principio de Le Châtelier es utilizado para poder valorar los efectos de estos cambios.
Formulación
Para la formulación del principio, Le Châtelier hizo referencia a dos importantes trabajos que ya habían sido realizados con anterioridad, uno de ellos hablaba sistemas de los que se encuentran en equilibrio debido a los cambios en la temperatura y el otro relacionado con la presión y la concentración. Châtelier demostró que con su enunciado buscaba la forma de incluir los fenómenos químicos que podían ser reversibles y formuló su principio de forma inductiva, sin tener aún ningún tipo de prueba teórica que respaldara su teoría.
Aplicaciones del principio de Le Châtelier
Este principio es aplicado principalmente en procesos industriales, pues en ellos es necesario conocer las condiciones que favorecen el desplazamiento de el equilibrio para poder formar un producto de manera adecuada para conseguir el mayor rendimiento en el proceso.
También es aplicado en el proceso de Haber, el cual es una ecuación química superior la cual corresponde a la formación del amoníaco, uno de los compuestos que se produce en grandes escalas industriales en donde las condiciones ideales para la obtención del NH3 son aquellas en la que la temperatura no sea muy elevada y en donde debe haber niveles altos de presiones. La naturaleza también utiliza el principio de Le Châtelier para recubrir de estalactitas los techos cavernosos.
Ejemplos
Algunos ejemplos del uso del principio de Le Châtelier son: en la síntesis orgánica, en la producción de gases licuados, en el transporte del oxígeno al cuerpo, en el equilibrio homeostático del cuerpo y en el proceso de la fotosíntesis.
¿Cómo citar este artículo?
Briceño V., Gabriela. (2018). Principio de Le Châtelier. Recuperado el 4 enero, 2025, de Euston96: https://www.euston96.com/principio-le-chatelier/